Nature子刊丨深圳先进院脑所/深港脑院张淑雯联合揭示自闭症相关SHANK3蛋白无序区介导相分离与突触可塑性的机制
SHANK3是公认的自闭症谱系障碍中最显著的风险基因之一,早期研究表明它对突触后致密区(PSD)的结构和功能至关重要,并且参与长时程可塑性增强(LTP)——即学习和记忆的基础。然而,SHANK3 究竟如何精确调控 LTP、如何响应神经元活动并以如此高的精度重塑 PSD,其分子机制仍未清楚解开。
4月20日,中国科学院深圳先进技术研究院脑认知与脑疾病研究所/深港脑科学创新研究院张淑雯团队联合医工所黄良宇团队在Nature Communications杂志上发表题为“Dynamic recruitment of CaMKII into SHANK3 phase-separated condensates tunes postsynaptic density remodeling during long-term potentiation”的研究论文。该研究突破性的通过引入液-液相分离这一生物物理概念,为上述问题提供了新的答案。研究团队发现,在突触激活后,LTP 中的关键激酶CaMKII会被迅速招募到位于树突棘的 SHANK3相分离凝聚体中,进一步作用于其下游靶点AMPAR受体,从而介导PSD的结构和功能重塑,最终实现突触传递的增强。这一发现巧妙地将分子遗传学、生物物理学和细胞神经科学联系起来,揭示了一个与自闭症相关的基因如何在机制上驱动活动依赖性的神经可塑性。

文章上线截图,文末链接可查看原文
SHANK3通过其内在无序区域介导了液相分离。全长的SHANK3能形成动态的凝聚体,但缺失IDR3(尤其是IDR3-3亚区区域)会严重削弱这一能力,而缺失IDR1、IDR2、IDR3-1或IDR3-2则无显著影响。简化版的SHANK3虽然能够相分离,但凝聚体性质不同于全长蛋白。
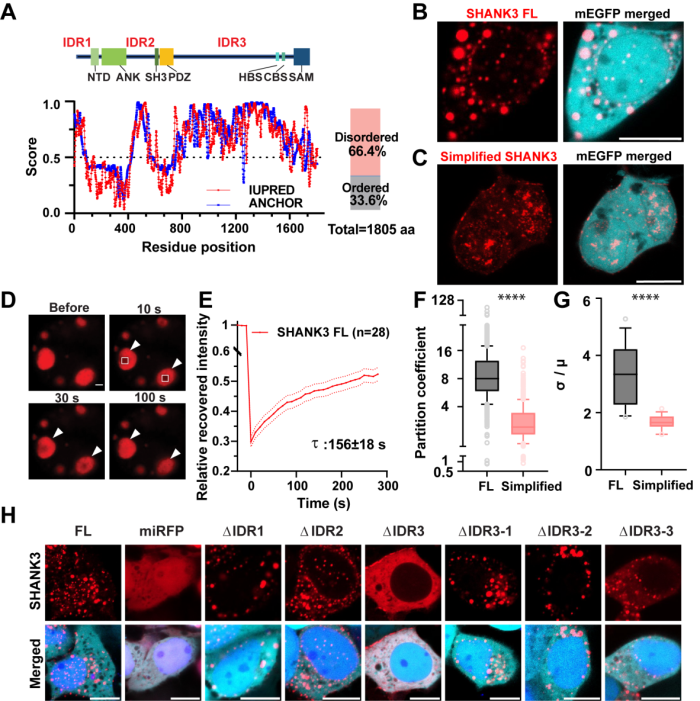
图1. SHANK3蛋白无序区介导液相分离的发生
在Shank3b敲除神经元中,全长SHANK3强定位至树突棘并维持静息态中正常PSD体积和AMPAR表达。缺失IDR3或其亚区IDR3-3会削弱SHANK3在树突棘中的富集、让PSD体积缩小并降低GluR1水平。有趣的是,ΔIDR3-1虽能高定位至树突棘,却无法恢复PSD大小,提示存在相分离以外的额外机制。
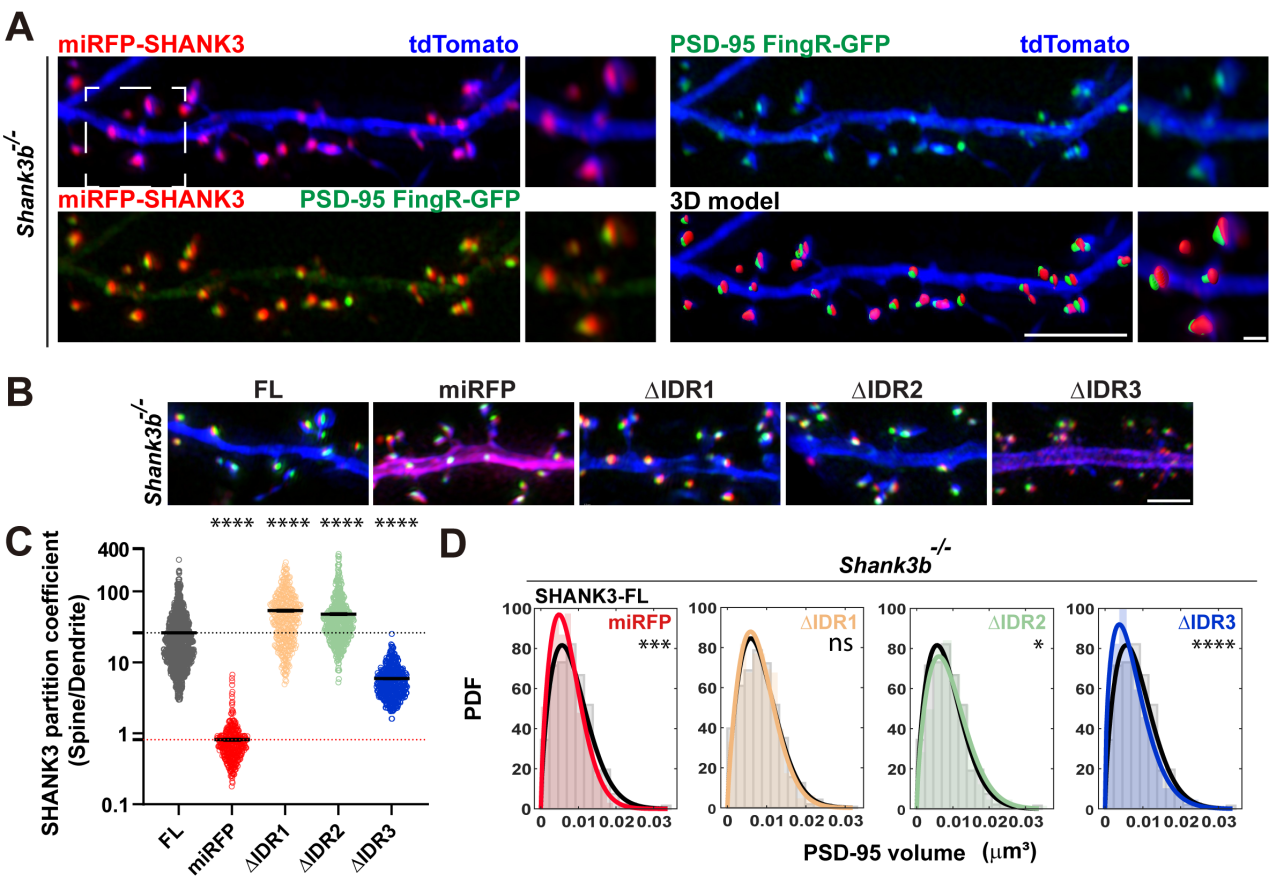
图2.SHANK3蛋白无序区缺失减少了它在树突棘上的富集,导致静息态的PSD体积缩小
CaMKII在钙内流或光刺激下被快速招募至SHANK3凝聚体中,进一步加速凝聚体融合与PSD重塑。研究人员使用了活细胞成像技术、相分离生物物理测定,对这一动态招募过程进行了详细描绘,验证了招募过程需要CaMKII自身磷酸化以及SHANK3的IDR3区域,尤其是IDR3-1亚区内的RRK基序。这一发现强调了CaMKII与SHANK3凝聚体相互作用在突触可塑性中的重要作用。
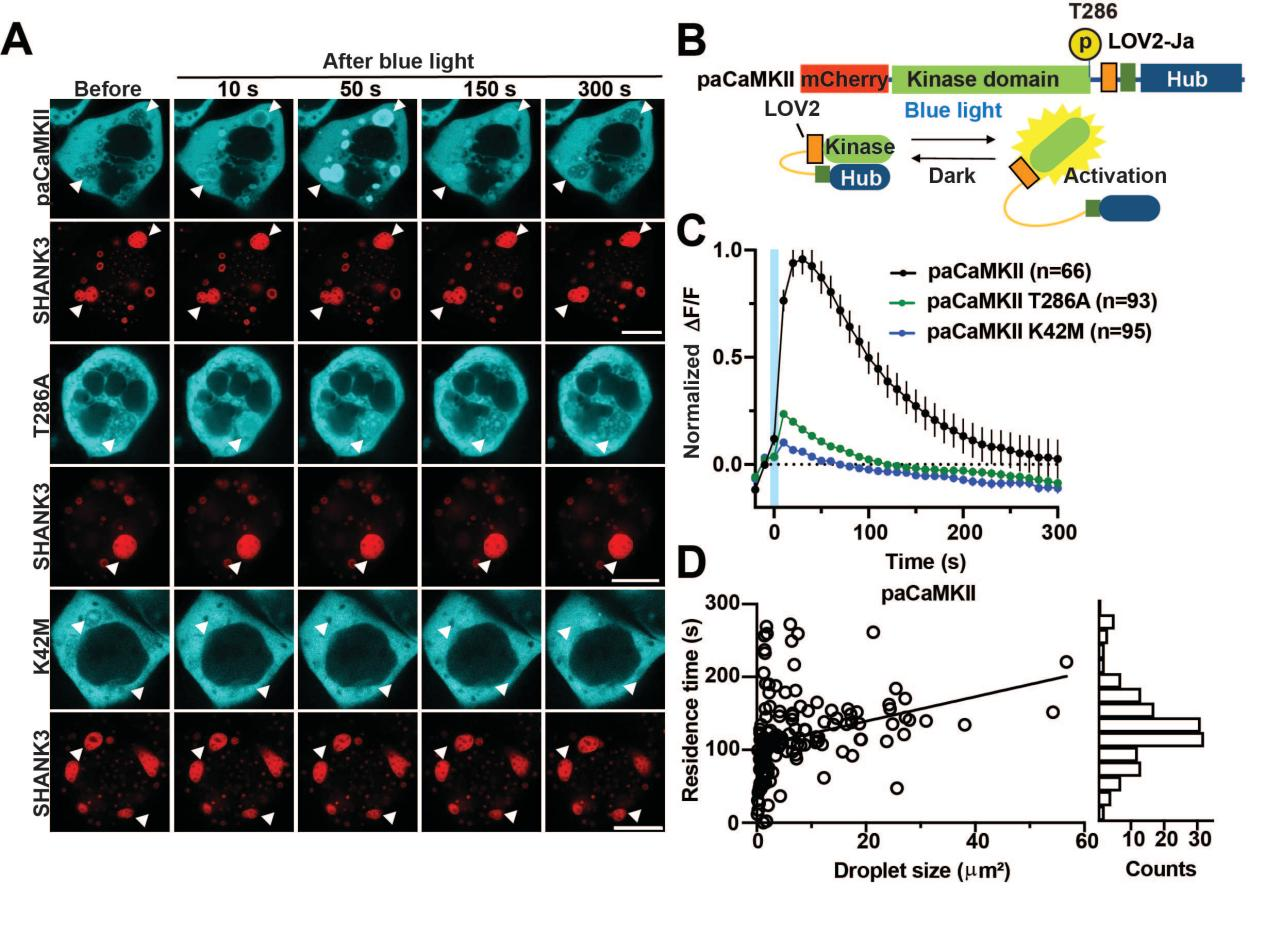
图3. 光调控CaMKII显示SHANK3凝聚体快速招募激活后的CaMKII
此次研究还揭示了与人类自闭症相关的SHANK3突变(InsG3680),这种突变导致SHANK3的部分IDR3以及SAM结构域的缺失,抑制了SHANK3的液相分离功能,造成了PSD重塑和AMPAR招募的缺陷。此结果为自闭症等神经发育障碍的分子机制提供了新的线索,并为未来的治疗策略开辟了新的方向。
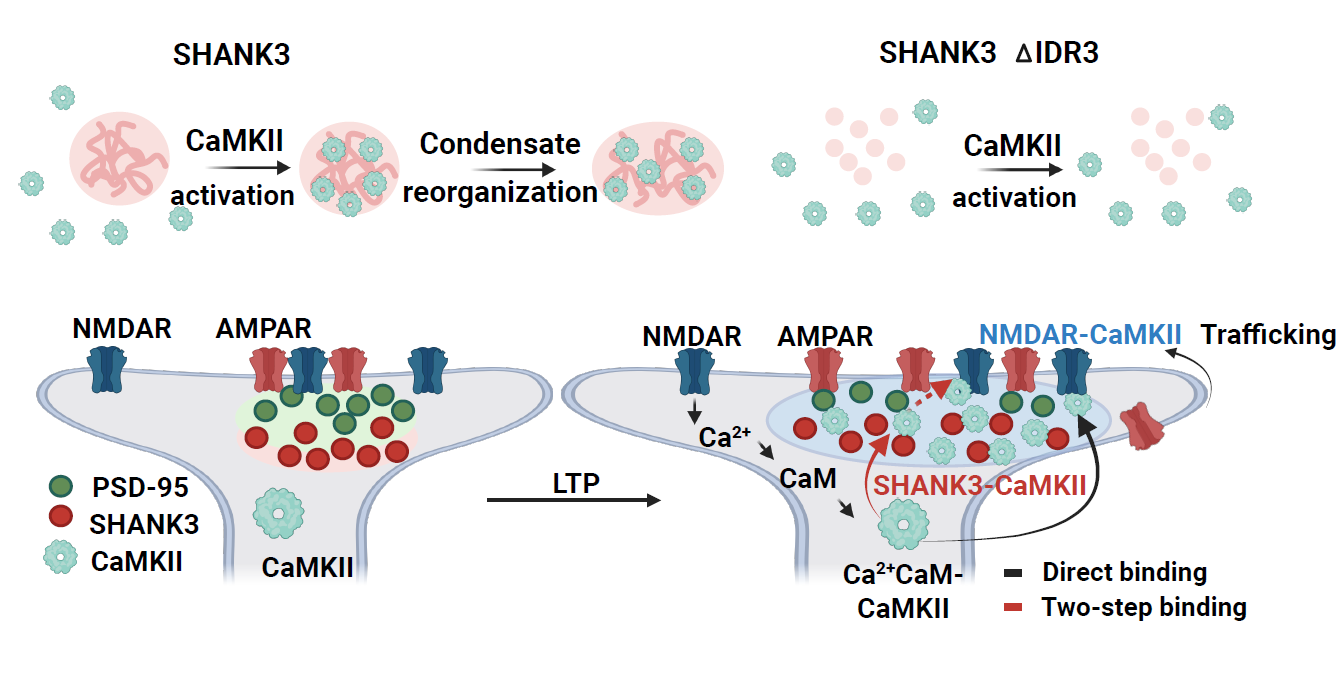
图4. SHANK3相分离介导突触长时程可塑性的机制模型
SHANK3通过CaMKII调控其凝聚体动力学,是LTP过程中PSD重塑的核心机制之一。这一发现不仅揭示了突触可塑性的全新分子机制,也为自闭症及其他神经发育障碍的潜在治疗靶点提供了新方向。SHANK3突变引起的自闭症和智力障碍,可能通过改变SHANK3的相分离特性,从而影响CaMKII的招募,调控突触强度并介导PSD的动态重塑。这项研究为在病理条件下调节突触功能提供了具体的分子靶点,也为开发针对神经功能障碍的新型治疗策略奠定了基础。
本研究通讯作者为深圳先进院张淑雯項目研究员与黄良宇副研究员,刘茜助理研究员是本研究工作的第一作者。该项目受到中国科学院、国家自然科学基金委、广东省科技厅、深圳市科创委等资助。感谢深港脑科学创新研究院以及深圳市脑解析与脑模拟重大科技基础研究设施对本研究的支持。
论文链接: